Illumina-DNA&RNA共建库试剂盒
产品介绍
Illumina-RNA&DNA共建库试剂盒是Illumina测序平台的DNA&RNA测序文库构建试剂盒,包含RNA反转录试剂,常规dscDNA合成试剂,DNA片段化试剂,接头连接试剂,以及文库扩增试剂。本产品利用专业开发设计的新一代片段化酶可以完成DNA和RNA一管式建库,简化了操作流程,极大的降低了建库时间和成本。本试剂盒具有优秀的文库转化率,可应用于mNGS样本,肿瘤样本,复杂样本等的建库。经测序验证,不同GC含量的样本,均可获得优异的测序结果,文库覆盖度高,均一性好,偏好性低,使建库变得更加简单高效。提供的所有试剂都经过严格的质量控制和功能验证,最大程度上保证了文库构建的稳定性和重复性。
产品优势
■ 利用专业开发设计的新一代片段化酶可以完成DNA和RNA一管式建库,简化了操作流程,极大的降低了建库时间和成本。
■ 文库覆盖度高,均一性好,偏好性低,使建库变得更加简单高效。
产品组分
|
名称 |
96T |
|
dT23VN |
96 μl |
|
Random Primer |
96 μl |
|
1st Reaction Buffer |
768 μL |
|
1st Strand Enzyme Mix |
192 μL |
|
2nd Reaction Buffer |
288 μL |
| 2nd Strand Enzyme Mix |
960 μL |
| Smearase Enzyme Mix | 480 μL |
| Ligation Enhancer | 2×1440 μL |
| Novel T4 DNA Ligase | 480 μ |
| 2×Super Canace | 1200 μL |
| Primer Mix | 480 μL |
注意事项
1.运输与保存方法:干冰运输。-20℃保存。有效期1年。
2.关于操作
■ 为了您的安全和健康,请穿实验服并戴一次性手套操作。
■ 请于使用前将试剂盒各组分置于室温解冻。解冻后上下颠倒数次充分混匀,短暂离心后置于冰上待用。
■ 推荐在带热盖的PCR仪中进行各步骤反应,使用前应预热PCR仪至反应温度附近。
■ 请使用无RNase污染的耗材,并对实验区域定期进行清理,推荐使用ThermoFisher公司的RNAZapTM高效核酸去除喷雾去除RNA酶污染。
■ PCR产物因操作不当极容易产生气溶胶污染,进而影响实验结果准确性。推荐将PCR反应体系配制区和PCR产物纯化检测区进行强制性的物理隔离;配备文库构建专用移液器等设备;定时对各实验区域进行清洁(推荐使用ThermoFisher公司的DNAZapTM高效核酸去除喷雾),以保证实验环境的洁净度。
■ 本产品仅作科研用途!
3.关于接头连接(Adapter Ligation)
■ 试剂盒标配接头:Index Kit V2 for Illumina。
■ 我们建议选用高质量的商业化接头。如客户使用自制接头,请委托具有NGS引物合成经验的公司,并备注需进行严格的防污染控制。此外,进行接头退火操作时,请在超净台完成。每次只操作一种接头,防止交叉污染。
■ 使用接头时,请提前将接头取出放在4°C或冰盒上解冻;在室温操作时,实验室温度最好不要超过25°C,防止接头解链。
■ 建库过程中,接头浓度过高或过低都会导致建库成功率变低。本试剂盒操作方案中,所加入的接头体积固定为5 μL,请根据初始的DNA或者RNA投入量,参考表1,表2对接头进行稀释。本公司接头原始浓度均为15 μM,接头稀释液请选择0.1×TE buffer,稀释过的接头可在4°C保存48小时。
表1. Input Total RNA量与接头使用浓度推荐表
|
Input Total RNA |
Adapter stock concentration |
|
10 ng |
1 μM |
|
100 ng |
1.5 μM |
|
500 ng |
3 μM |
|
≥1 μg |
5 μM |
表2. Input Total DNA量与接头使用浓度推荐表
|
Input Total DNA |
Adapter stock concentration |
|
1μg~200 ng |
15 μM |
|
100 ng |
10 μM |
|
500 ng |
5 μM |
|
10 ng |
3 μM |
| 5 ng | 1.5 μM |
| 1 ng | 1 μM |
4.关于文库扩增(Library Amplification)
■ 本试剂盒中的文库扩增组分由本公司第二代高保真 DNA 聚合酶所组成,在第一代的基础上,大大增强了扩增的均一性,即使是低拷贝的基因,也能进行无偏好性地扩增。
■ 如果您使用 Indexed Adapter(也称为长接头、大 Y 接头),可使用本试剂盒提供的引物 Primer mix 进行扩增;如果使用的是“短接头”或者叫“小 Y 接头”,则需要使用 Index Primers 进行扩增,加上相应的 Index。
■ 文库扩增步骤需要严格控制扩增循环数。循环数不足,将导致文库产量低;循环数过多,又将导致文库偏好性增加、重复度增加、嵌合产物增加、扩增突变积累等多种不良后果
5.DNA磁珠纯化与分选(Bead-based Clean Up and Size Selection)
■ 建库过程中有多个步骤需要使用DNA纯化磁珠,我们推荐使用th DNA Selection Beads (th Cat#)进行DNA纯化和分选。
■ 磁珠使用前应先平衡至室温,否则会导致得率下降、分选效果不佳。
■ 磁珠每次使用前都应充分振荡混匀或使用移液器上下吹打充分混匀。
■ 转移上清时,请勿吸取磁珠,即使微量残留都将影响后续文库质量。
■ 磁珠洗涤使用的80%乙醇应现用现配,否则将影响回收效率。
■ 产物洗脱前应将磁珠置于室温干燥。干燥不充分容易造成无水乙醇残留影响后续反应;过分干燥又会导致磁珠开裂进而降低纯化得率。通常情况下,室温干燥3-5 min足以让磁珠充分干燥。
■ DNA纯化或长度分选产物如需保存,可使用0.1×TE Buffer洗脱,产物于4°C可保存2天,-20°C可保存1个月。
6.关于文库质检(Library Quality Analysis)
■ 通常情况下,构建好的文库可通过长度分布检测和浓度检测来进行质量评价。
■ 文库浓度检测可使用:基于双链DNA荧光染料的方法,如Qubit®、PicoGreen®等;基于qPCR绝对定量的方法。
■ 推荐使用qPCR方法进行文库浓度检测:Qubit®等基于双链DNA荧光染料的浓度测定方法时,无法有效区分单端连接Adapter的产物、两端均未连接Adapter的产物及其他不完整双链结构产物;qPCR绝对定量基于PCR扩增原理,仅定量样品中两端Adapter完整的文库(即可测序的文库),可排除单端或双端都不连接Adapter的不可测序文库的干扰。
■ 文库浓度检测不可使用:基于光谱检测的方法,如NanoDrop®等。
■ 文库长度分布检测,可通过Agilent Bioanalyzer 2100等基于毛细管电泳或微控流原理的设备进行检测。
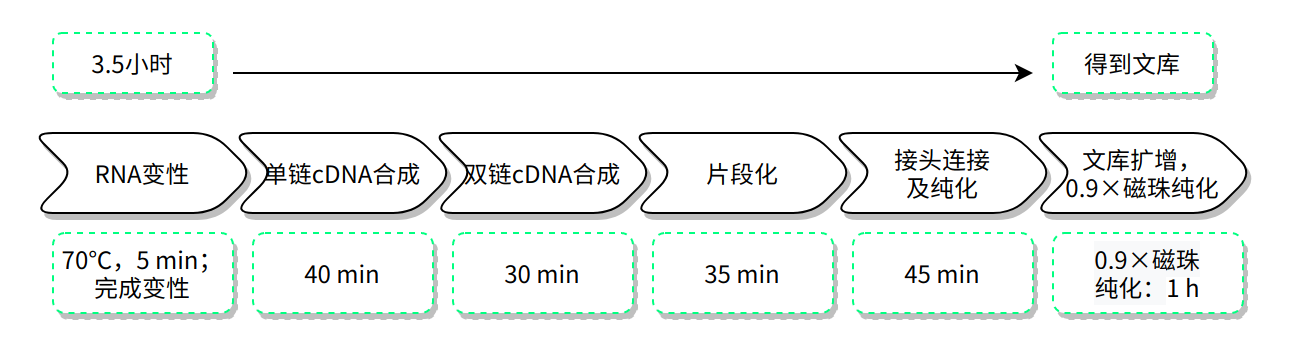
操作流程